Profilaxis Pre- exposición para la prevención del VIH en mujeres

 AUTORES:
AUTORES:
Luciana Spadaccini a, Omar Sued b
Sobre los autores
- Médica especialista en enfermedades infecciosas. Sub-investigadora en fundación Huésped. Profesora de Microbiología de la UBA. Miembro de la comisión de sida y ETS de la Sociedad Argentina de Infectología.
- Médico especialista en enfermedades infecciosas. Doctor en Medicina. Director del área de investigaciones en Fundación Huésped. Presidente de la Sociedad Argentina de Infectología.
Introducción
En Argentina se estima que 139.000 personas viven con VIH, por año se notifican 5.800 casos nuevos, los cuales la mayoría (68%) ocurren en hombres. El 98% de las infecciones se producen por relaciones sexuales sin protección: en los hombres el 56,3% ocurre por relaciones sexuales con otros hombres y el 42 % por relaciones sexuales con mujeres; en mujeres, sin embargo, el 97,1% de las infecciones ocurre por relaciones sexuales con hombres. 1
En mujeres, los nuevos diagnósticos de VIH ocurren principalmente en el grupo etario de 25-34 años, seguido por el grupo de 35-44 años. Con respecto al nivel de instrucción alcanzado al momento del diagnóstico, el 43 % de las mujeres que se infectan han terminado o superado la educación media 1.
La prevalencia del VIH es mucho más alta en determinadas subpoblaciones, siendo de 34% en mujeres transgénero, de 12 a 15 % en hombres que tienen sexo con hombres (HSH) y de 2 a 5% en trabajadores/as sexuales (en comparación con el 0,4 % en jóvenes y adultos de la población general )1 En estas subpoblaciones es donde se concentran los sujetos en alto riesgo de adquirir la infección por VIH y que son los candidatos a recibir la profilaxis pre- exposición (PrEP).
El tratamiento antirretroviral (TARV) en las personas que viven con VIH, previene el descenso de los linfocitos T CD4 (reduciendo la incidencia de enfermedades oportunistas) y evita la replicación viral, disminuyendo las copias virales por ml de sangre hasta niveles que no pueden ser detectados por los análisis convencionales, lo que se denomina “carga viral indetectable¨ 2. Además de este efecto individual en la morbimortalidad de las personas con VIH, el TARV tiene un gran impacto poblacional al disminuir la carga viral comunitaria, es decir la cantidad de personas que pueden transmitir la infección a través de las relaciones sexuales; esto se conoce como Tratamiento como prevención del VIH y se basa en el concepto I=I (Indetectable = Intransmisible). Este concepto nace en 2016, respaldado por múltiples estudios clínicos 3, 4, 5, 6 que avalan la ausencia de transmisión sexual del VIH en personas que están en tratamiento antirretroviral de manera continua y con carga viral indetectable por más de 6 meses. Esto es de gran importancia a nivel individual, ya que permite a las parejas en las que uno de los miembros tiene VIH y el otro no (parejas serodiscordantes), reiniciar relaciones sexuales no protegidas sin riesgo de transmisión, mejorando la intimidad de la pareja, reduciendo el miedo y la ansiedad, disminuyendo el estigma y permitiendo la planificación familiar. Es importante mencionar que si bien el concepto I=I se refiere exclusivamente a la transmisión por vía sexual2 tiene un importante impacto en la transmisión materno infantil del VIH, ya que la carga viral materna es el factor de riesgo más importante para la transmisión del VIH a un recién nacido. Sin embargo, la evidencia científica actualmente disponible no permite extrapolar el I=I a la transmisión perinatal (post-parto o lactancia) ni al uso de jeringas u otros materiales cortopunzantes.2
Para materializar los efectos del tratamiento como prevención, la OMS propuso para el año 2020 un ambicioso objetivo para contribuir al fin de la epidemia de sida, que se conoce como los tres 90: 1) que el 90% de las personas que viven con VIH conozcan su diagnóstico, 2) que el 90% de las personas diagnosticadas con VIH reciban TARV y c) que el 90% de las personas que reciben tratamiento estén indetectables. La modelización sugiere que lograr estos objetivos antes de 2020 permitirá a la comunidad mundial acabar con la epidemia de sida en 2030.
¿Cómo lograr el 90/90/90?
La expansión masiva de testeo de VIH, la implementación de la Prevención combinada en aquellas personas en riesgo que son VIH negativas, y el inicio inmediato de TARV a las personas que tienen VIH son las principales medidas para lograr este objetivo.
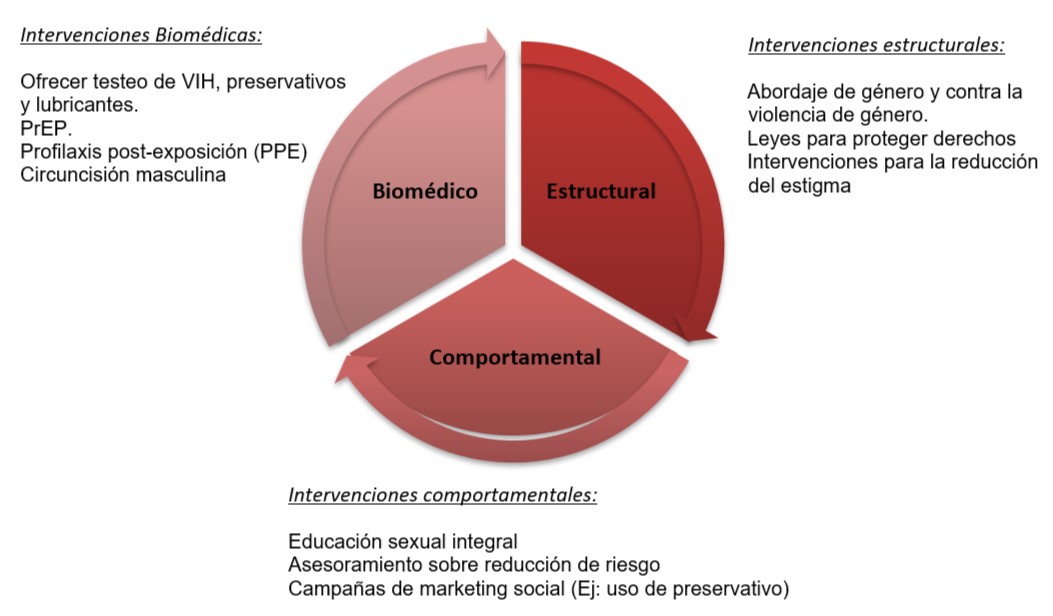
La Prevención combinada para las personas sin VIH pero que están en riesgo de adquirirlo es un conjunto de programas que combinan intervenciones biomédicas, comportamentales y estructurales, con el propósito de prevenir la infección por el VIH (Figura 1)
Figura 1. Prevención combinada del VIH
Que es la Profilaxis Pre-Exposición
La profilaxis pre exposición (PrEP) es una intervención prometedora para prevenir la adquisición del VIH. Tiene beneficios tanto individuales como a nivel de la salud de la población y es una valiosa herramienta para complementar los esfuerzos de salud pública para eliminar el VIH. A su vez, también sirve como puerta de entrada para acceder a servicios de salud sexual y reproductiva.
La PrEP se refiere al uso de antirretrovirales en personas VIH negativas que tienen alto riesgo de contraer el virus. La OMS propone esta estrategia en subpoblaciones que tienen una incidencia de VIH del 3% anual, y que en general son los HSH, las mujeres transgénero, las/os trabajadoras/es sexuales y las personas que tienen parejas VIH positivas que no tienen la carga viral indetectable.
El objetivo de la PrEP consiste en lograr altas concentraciones de antirretrovirales en mucosas (oral, genital, rectal) y sangre para prevenir la infección en caso de exposición. Constituye una medida altamente costo efectiva cuando se aplica en poblaciones con riesgo significativo de adquirir VIH.
Al momento, la única medicación oral aprobada para el uso de PrEP en mujeres es el tenofovir/emtricitabina o Truvada®, su uso diario mostró una eficacia mayor al 95% en términos de reducción del riesgo de infección por VIH. Esta eficacia depende de la adherencia a la medicación7, ya que las concentraciones vaginales de tenofovir son 100 veces menores que las rectales. Es por ello que la PrEP debe administrarse de manera diaria en mujeres para ser efectiva (a diferencia de lo que ocurre en HSH donde la administración intermitente, Ej.: 4 veces por semana, ha demostrado ser protectora). 8
Articulada con otros componentes de la Prevención combinada (como la educación sexual integral, el uso de preservativos, la circuncisión masculina, la profilaxis post-exposición, etc.), la PrEP permite además un diagnóstico y tratamiento temprano de casos incidentales de otras infecciones de transmisión sexual (ITS).
La buena adherencia a la PrEP requiere no solo de un manejo adecuado por los propios individuos, sino que también debe tener en cuenta los factores sociales y contextuales, especialmente para las mujeres. El estudio de PrEP en mujeres africanas (FEM-PrEP) puso en evidencia el peso de las barreras culturales (como el estigma sobre actividad sexual) que en este estudio se asoció a una muy baja adherencia. Estos hallazgos resaltan la importancia de facilitar el acceso a los servicios de salud sexual y reproductiva, que aborden el riesgo de VIH con una mirada amplia, a fin de identificar mujeres en riesgo, que puedan ser escuchadas y acompañadas para asegurar una buena adherencia9 .
La PrEP es generalmente bien tolerada, pero se deben informar los posibles efectos adversos, dentro de los más frecuentes se presenta la cefalea, náuseas y dolor abdominal leve que habitualmente no requieren tratamiento y desaparecen espontáneamente dentro del primer mes. Asimismo, por el uso de tenofovir, se debe monitorear la función renal y riesgo de osteopenia-osteoporosis, en particular en las personas con factores de riesgo. En base a los estudios clínicos de PrEP, se constató que los efectos adversos sobre la función renal y la aparición de desmineralización ósea en caso de presentarse son reversibles con la suspensión de la profilaxis.
PrEP en mujeres
La complejidad de los factores asociados con el riesgo de contraer el VIH en las mujeres se ha caracterizado por mucho tiempo en la literatura y apunta a la interacción de predictores de riesgo biológicos, junto con factores socio- conductuales, estigma e inequidad socioeconómica10. Por ello, las mujeres no pueden ser consideradas como subpoblación de riesgo per se, sino que ante cada mujer deben evaluarse los determinantes sociales que incrementan la vulnerabilidad. Estos incluyen la falta de educación formal, la pobreza, el uso de drogas y la falta de acceso a los servicios de salud sexual y reproductiva. Desde el 2012, año en que la Administración de Drogas y Alimentos de los Estados Unidos (FDA) aprobó el uso de Truvada ® para PrEP, la Organización Mundial de la Salud (OMS) emitió una serie de recomendaciones basadas en la evidencia que consideran cómo ofrecer PrEP a las mujeres con riesgo sustancial de contraer el VIH11 .
Actualmente las recomendaciones de PrEP en mujeres incluyen a 8,12:
- Mujeres con múltiples parejas sexuales,
- Mujeres trabajadoras sexuales,
- Mujeres con al menos un episodio de sexo vaginal y/o anal receptivo sin uso de preservativo en los últimos seis meses con una pareja sexual con infección por VIH que no está indetectable.
En la práctica, muchas mujeres con una pareja VIH positiva consultan por la necesidad de recibir PrEP. En este contexto debe recordarse el concepto I=I y reforzar la necesidad de que la pareja tome la medicación en forma correcta, y se realice los controles en forma periódica (cada 4-6 meses) para asegurar que se encuentra indetectable, ya que la carga viral aumenta a los pocos días de suspender el tratamiento. El concepto I=I permite ofrecer a las parejas serodiscordantes la oportunidad de proceder a la concepción en forma natural si desean concebir. En consecuencia, en el caso de que una mujer VIH negativa desee concebir y su pareja VIH positiva este indetectable, no hay evidencia que la PrEP a la pareja VIH negativa reduzca aún más el riesgo de transmisión sexual. 13
En el caso de que una mujer VIH negativa desee concebir y su pareja VIH positiva no se encuentre indetectable, se puede utilizar PrEP como medida de protección de la mujer, y las guías recomiendan comenzar su uso un mes antes de la concepción y continuarlo hasta un mes después de la misma, limitando las relaciones sexuales sin preservativo al periodo periovulatorio. 14
La implementación de PrEP requiere de servicios de salud en condiciones de recibir a las poblaciones descritas previamente y con personal capacitado para ofrecer testeo basal y periódico de VIH, descartar infección por el virus de la hepatitis B (HBV), indicar vacunación y testeo de otras ITS, realizar consejería, provisión de preservativos y salud sexual orientada a diferentes grupos y edades, soporte para estrategias de reducción de daño, referencia a servicios de prevención de adicciones y soporte social. Dado que la adherencia es un factor clave en el éxito de la PrEP debe discutirse en profundidad este aspecto antes de recomendarla.
Es importante enfatizar que la PrEP, es una herramienta más de prevención dentro de la Prevención Combinada11 y para lograr el objetivo (prevenir nuevas infecciones) es importante actuar tanto sobre las intervenciones biomédicas, como las estructurales y comportamentales.
En nuestro país, la PrEP se encuentra aprobada por ANMAT, pero todavía no se proporciona en forma gratuita como una medida de salud pública. La Dirección de Sida, ETS, Hepatitis y Tuberculosis ha tomado recientemente la decisión de llevar a cabo un proyecto piloto de implementación de la PrEP en el contexto de la estrategia de Prevención Combinada, que estaría disponible durante el año 2020.
Bibliografía.
-
Boletín N° 36 sobre el VIH, sida e ITS en la Argentina, Diciembre 2019. Dirección de Sida, ETS, Hepatitis y TBC, Secretaría de Gobierno de Salud, Ministerio de Salud y Desarrollo Social. Argentina, 2019. http://www.msal.gob.ar/images/stories/bes/graficos/0000001754cnt-boletin-epidemiologico-2019-vih-sida-its.pdf
-
Documento de consenso de la Dirección de Sida, ETS, Hepatitis y TBC, Secretaría de Gobierno de Salud, Ministerio de Salud y Desarrollo Social. Argentina, 2019. http://www.msal.gob.ar/images/stories/bes/graficos/0000001546cnt-2019-08-28_indetectable-igual-intrasmisible.pdf
-
Cohen MS, Chen YQ, McCauley M, Gamble T, Hosseinipour MC, Kumarasamy N, et al. Antiretroviral Therapy for the Prevention of HIV-1 Transmission. N Engl J Med. 2016 Sep 1; 375(9):830–9.
-
Rodger AJ, Cambiano V, Bruun T, Vernazza P, Collins S, Lunzen J van, et al. Sexual Activity Without Condoms and Risk of HIV Transmission in Serodifferent Couples When the HIV-Positive Partner Is Using Suppressive Antiretroviral Therapy. JAMA. 2016 Jul 12;316(2):171–81.
-
Bavinton, B. Grinsztejn, N. Phanuphak, F. Jin, I. Zablotska, G. Prestage, et al. HIV treatment prevents HIV transmission in male serodiscordant couples in Australia, Thailand and Brazil. In 2017 [cited 2017 Aug 30]. Available from: http://programme.ias2017.org/Abstract/Abstract/5469
-
A. Rodger, V. Cambiano, T. Bruun, P. Vernazza, S. Collins, G.M. Corbelli, et al. Risk of HIV transmission through condomless sex in MSM couples with suppressive ART: The PARTNER2 Study extended results in gay men. In Amsterdam, Netherlands.; 2018 [cited 2018 Aug 30]. Available from: https://onlinelibrary.wiley.com/doi/ epdf/10.1002/jia2.25148
-
Baeten JM, Donnell D, Ndase P, Mugo NR, Campbell JD, Wangisi J, et al. Antiretroviral prophylaxis for HIV prevention in heterosexual men and women. New England Journal of Medicine. 2012; 367(5):399–410.
-
VII Consenso Argentino de Terapia Antirretroviral 2018-2019, Sociedad Argentina de Infectología, Comisión de SIDA y ETS.
-
Yun K, Xu JJ, Zhang J, Li JM, Hu QH, Chu ZX, Jiang YJ, Geng WQ, Shang H, Wang N.Female and younger subjects have lower adherence in PrEP trials: a meta-analysis with implications for the uptake of PrEP service to prevent HIV. Sex Transm Infect. 2018 May;94(3):163-168
-
Hodges-Mameletzis I, Fonner VA, Dalal S, Mugo N, Msimanga-Radebe B, Baggaley R. Pre-Exposure Prophylaxis for HIV Prevention in Women: Current Status and Future Directions. Drugs. 2019 Aug; 79(12):1263-1276
-
UNAIDS. Data 2018 Report, Joint United Nations Programme on HIV/AIDS (UNAIDS), 2018
-
Who implementation tool for pre-exposure prophylaxis of HIV infection. Julio 2017.
-
Davies N, Heffron R. Global and national guidance for the use of pre-exposure prophylaxis during peri-conception, pregnancy and breastfeeding. Sex Health. 2018 Nov;15(6):501-512
-
Panel on Treatment of Pregnant Women with HIV Infection and Prevention of Perinatal Transmission. Recommendations for Use of Antiretroviral Drugs in Transmission in the United States. Available at http://aidsinfo.nih.gov/ contentfiles/lvguidelinesPerinatalGL.pdf. Accessed 12 October 2019 .




