Dispositivo Liberador de Levonorgestrel: ¿Cuál es su Lugar en el Sangrado Uterino Anormal?
Autor
Dr. David Escobar Paredes
Cirugía Endoscópica Ginecológica
Profesor Adjunto Universidad de Chile
FACOG, MBA© en Salud
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.
Introducción
Las alteraciones en el sangrado menstrual tienen sus definiciones precisas, pero no existe un término apropiado para el concepto general. Si bien estas alteraciones podrían semánticamente ser denominadas como metrorragia, este término se asocia equivocadamente con cantidad. Es por esto que en la literatura extranjera se utiliza el concepto de Abnormal Uterine Bleeding (AUB), Sangrado uterino anormal (SUA), para englobar a todas las alteraciones de frecuencia y cantidad en relación a flujo rojo, excluyendo causas relacionadas con embarazo y patología de cuello uterino. Recientemente la FIGO ha adoptado la terminología (PALM-COEIN) para agrupar todas las entidades etiológicas del SUA (1)
El SUA constituye uno de los principales motivos de consulta en ginecología y es responsable de una importante proporción de procedimientos diagnósticos y quirúrgicos que la mayoría de las veces culmina en la histerectomía. La histerectomía es una solución definitiva, aunque no siempre justificada, pues es conocido que al revisar las piezas quirúrgicas enviadas a anatomía patológica solo en un 50 % de ellas se observa evidencia de enfermedad orgánica.
En EEUU se realizan 600.000 histerectomías anuales. Se estima que en este país, un 35 % de las mujeres están histerectomizadas antes de los 65 años contrastando por ejemplo con el 15 % de mujeres histerectomizadas antes de los 70 años en Italia, país que cuenta con un sistema de salud más social, lo que hace evidente también un trasfondo económico en la toma de decisiones.
En la última década se han sumado nuevas alternativas, tanto para mejorar el diagnóstico como para ofrecer tratamientos médicos y quirúrgicos más racionales que ayuden en su conjunto a evitar histerectomías innecesarias. Esta propuesta pretende presentar ordenadamente las alternativas hoy disponibles y mostrar una sugerencia de algoritmo de manejo del SUA.
Diagnóstico en SUA
La clínica, ecotomografía transvaginal (ECO TV) y estudio histológico de material endometrial obtenido mediante legrados uterinos han demostrado con el paso del tiempo ser insuficientes para tomar una conducta correcta respecto al SUA. Ejemplo de esto es el alto porcentaje de falsos positivos de la ECO TV en el diagnóstico de patología endouterina (2) y el alto porcentaje de posibles falsos negativos del legrado uterino. La ECO TV tiene un rol indiscutido en la ginecología pero no siempre es capaz de identificar patología intracavitaria focal. Respecto al legrado uterino debemos recordar que es solamente una toma de muestra endometrial, es un procedimiento ciego, y que en el 60 % de los casos solo se logra legrar menos del 50 % de la superficie de la cavidad endometrial. Además, de las muestras obtenidas hasta un 30 % es insuficiente para diagnóstico anatomopatológico(3). Estas situaciones evidencian la necesidad contar con nuevos elementos de apoyo al diagnóstico del SUA.
El desarrollo de ópticas y su utilización en otras áreas de la medicina hicieron posible la incorporación de la histeroscopía como una importante herramienta en la evaluación y tratamiento de la paciente con SUA. En efecto, con la histeroscopía diagnóstica (HCP) se logra una óptima visualización de la cavidad uterina, y de esta forma es posible establecer con una alta probabilidad la causa del SUA. Los informes histeroscópicos son sugerentes de una determinada patología, pues es la histología quién continua entregando la certeza diagnóstica. La HCP siempre debe ir acompañada de una biopsia dirigida, con la sola excepción de la Atrofia Endometrial. La HCP ha demostrado ser un examen confiable, con pocas contraindicaciones y complicaciones, y que entrega valiosa información en problemas ginecológicos frecuentes. En la actualidad, gracias a la introducción de ópticas más finas (2,9 mm), es posible contar con histeroscopios con canal de trabajo los cuales no superan los 5 mm de diámetro y que permiten entre otras cosas: toma de muestras directas para el estudio histológico, resección de pequeños pólipos endometriales, cateterización tubaria para esterilización, lisis de sinéquias y extracción de DIU.
La ultrasonografía, por su parte, también ha logrado notables avances. El primero de ellos es el aporte de la histerosonografía (HSG), la cual al distender la cavidad uterina y separar las paredes aumenta notablemente sus resultados diagnósticos acercándola a la histeroscopía, sobretodo en diagnósticos de pólipos y miomas, aunque difícilmente en anormalidades endometriales menos aún en aquellas focales. El uso de la ecotomografía tridimensional (ECO 3D) también es un aporte interesante en el diagnóstico de causas orgánicas del SUA aunque sin duda es la histerosonografía tridimensional (HSG 3D) la cual podría igualar la sensibilidad y especificidad de la HCP. No obstante lo anterior, es importante resaltar que el gold standard para todos estos procedimientos diagnósticos sigue siendo la anatomía patológica, y que para establecer la capacidad diagnóstica de cualquiera de ellos es fundamental determinar la forma en que se obtiene el material para estudio histológico y así evitar las disparidades de resultados que se observan en la actualidad. Si la HCP es o no superior a HSG, ECO 3D o HSG 3D en el diagnóstico de patología endouterina, no debe ser materia de discusión, pues todos estos exámenes persiguen el mismo objetivo, identificar patología focal. Su utilización dependerá de los medios y experiencia disponibles en cada centro.
Tratamiento en SUA
Una vez realizada la evaluación diagnóstica señalada -excluidas las neoplasias cuyo tratamiento escapa a los objetivos de esta propuesta- los caminos terapéuticos son tres: Tratamiento farmacológico en base a cualquiera de las alternativas actuales; Tratamiento quirúrgico ablativo focal (cirugía conservadora); y Tratamiento quirúrgico no conservador, básicamente histerectomía en cualquiera de sus formas.
Tratamiento farmacológico: Existen distintas alternativas, todas ellas comparadas en múltiples publicaciones, existiendo revisiones en el Cochrane que esclarecen las mejores opciones para el manejo. En estas publicaciones se ha establecido que el uso de ácido tranexámico provoca una mayor reducción en las mediciones objetivas del SUA en comparación a placebo u otros tratamientos médicos -específicamente antinflamatorios no esteroidales (AINEs) y progestágenos cíclicos- además de provocar menos efectos colaterales. Los AINEs reducen significativamente el SUA en comparación a placebo, pero son menos eficaces que antifibrinolíticos, y sin diferencias al compararlos con anticonceptivos (ACOs) y progestágenos cíclicos. Los progestágenos cíclicos, administrados desde el día 15 o 19 hasta el 26, no ofrecen ventajas sobre ACOs y AINEs y solo tendrían utilidad en el manejo a corto plazo del SUA. No existen revisiones en relación a progestágenos de depósito que si tienen importancia en el tratamiento de hiperplasias endometriales sin atipias (4, 5 ,6).
Mención aparte merece la utilización del dispositivo intrauterino con 52 mg de levonorgestrel en su rama vertical, que libera 20 microgramos de esta progestina diarios por al menos 5 años (DIU-LNG, Mirena®, Bayer S.A.). Si bien es un DIU con indicación de anticonceptivo, produce una intensa atrofia endometrial mediante la reducción de la expresión de los receptores de estrógenos y progesterona endometriales, entre alguno de los mecanismos comprobados. Numerosas publicaciones internacionales y algunas nacionales (7, 8) demuestran su utilidad en el manejo del SUA. De acuerdo a revisiones recientes, el DIU-LNG es superior al tratamiento con progestágenos cíclicos, y superior a los otros tratamientos médicos en el largo plazo considerando las pérdidas hemáticas y la satisfacción de la usuaria (9). El DIU-LNG tiene esta segunda indicación (SUA) aprobada en más de 110 países. EL DIU-LNG es la primera elección en SUA en guías NICE del Reino Unido, demostrando además la mejor relación costo-efectividad en el manejo del SUA. (10)
Existe un grupo especial de pacientes en las cuales la indicación del DIU-LNG es perentoria: pacientes de alto riesgo quirúrgico. Al respecto es interesante mencionar nuestra experiencia (8) con la utilización de este DIU, con criterios específicos (Tabla 1), como alternativa a la histerectomía en este grupo de pacientes (ASA 2 y 3). En ella se usa DIU-LNG en cardiópatas, nefrópatas, trastornos de coagulación, obesas mórbidas, demostrando una objetiva disminución de la metrorragia de acuerdo a Pictorial Charts (11) utilizando como índice de menorragia un score mayor a 185 puntos. Este hecho es de gran importancia considerando las distintas frecuencias de mortalidad perioperatoria reportadas en relación a la clasificación de la Sociedad Americana de Anestesia.
Tabla 1 Criterios de inclusión y exclusión de DIU-LNG en SUA
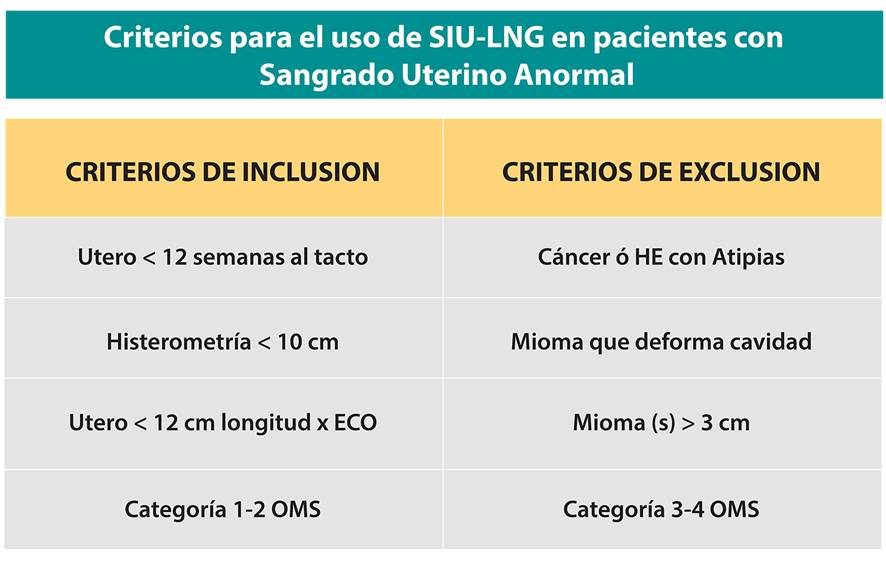
Tratamientos quirúrgicos conservadores: Hasta 30 % de los SUA son causados por Pólipos Endometriales (PE) o Miomas Submucosos (MS) y es por esto que es el resectoscopio el instrumento central en el manejo quirúrgico conservador del SUA. La resección histeroscópica es la intervención quirúrgica menos invasiva y de más rápida recuperación en SUA, con tiempos quirúrgicos promedio que difícilmente exceden los 30 minutos. Sus resultados a largo plazo son excelentes y sin duda pueden evitar muchas histerectomías que en estos casos claramente es un sobre-tratamiento (12).
Otra posibilidad quirúrgica que ofrece la histeroscopía quirúrgica es la Ablación o Resección Endometrial (RE) que consiste en la remoción del endometrio y miometrio superficial. Está indicada en mujeres con paridad completa, refractarias a tratamiento médico, en úteros de mediano volumen y sin patología neoplásica. Esta técnica en manos competentes resulta exitosa en el manejo del SUA en el 90 % de los casos (13).
Existen otros métodos ablativos puros: Ablaciones con Laser-técnica touch y non touch- y la Ablación con roller ball, que en conjunto con la RE son denominados métodos ablativos de primera generación. Si bien sus resultados son similares, la RE tiene la gran ventaja de proveer mucho material el cual puede ser estudiado histológicamente a diferencia de los otros métodos ablativos. La gran desventaja de los tres es que requieren de experiencia. Por esta razón se idearon otros métodos con curva de aprendizaje menor: Ablación térmica, Ablación con radiofrecuencia y Crioablación (métodos ablativos de segunda generación). Estos últimos son más fáciles de realizar, requieren de menor experiencia endoscópica pero sus resultados no superan a la RE, la cual sigue siendo el gold standard de acuerdo a revisión del Cochrane (14).
Una revisión sistemática de estudios clínicos aleatorizados comparó la ablación con el DIU-LNG para el tratamiento de mujeres con SUA. A los 6 meses, el DIU-LNG había reducido la pérdida sanguínea tanto como la ablación, y las reducciones persistieron a los 12 y 24 meses. La tasa de fallas fue similar y ambos métodos produjeron mejorías similares en la calidad de vida. Sin embargo, las usuarias del DIU-LNG no necesitaron otro método anticonceptivo por separado (15). Considerando que el DIU-LNG tiene la misma efectividad que los métodos ablativos de endometrio con la ventaja adicional de ofrecer anticoncepción y mejor relación costo-efectividad, se excluyen de esta propuesta de manejo los métodos ablativos endometriales.
Tratamiento quirúrgico no conservador: 20 años atrás este consistía básicamente en la Histerectomía Abdominal (HA) y la Histerectomía vaginal (HV), siendo esta última reservada solo para aquellas pacientes con prolapso genital completo. Desde entonces se comenzó a realizar la HV en pacientes sin prolapso, renovándose el interés por la cirugía vaginal. Contemporáneamente irrumpe la Laparoscopía en Ginecología. A finales de los 80 se publica la primera Histerectomía por vía laparoscópica (HL) y de ahí en adelante sus variaciones por ej. Histerectomía Vaginal asistida por Laparoscopía (HVAL). Una variante de la HA clásica es la HA por minilaparotomía utilizando un anillo de silicona que separa atraumáticamente los tejidos. Este anillo diseñado para minilaparotomías (3 a 9 cm) permite un campo operatorio reducido, pero óptimo para cirujanos experimentados.
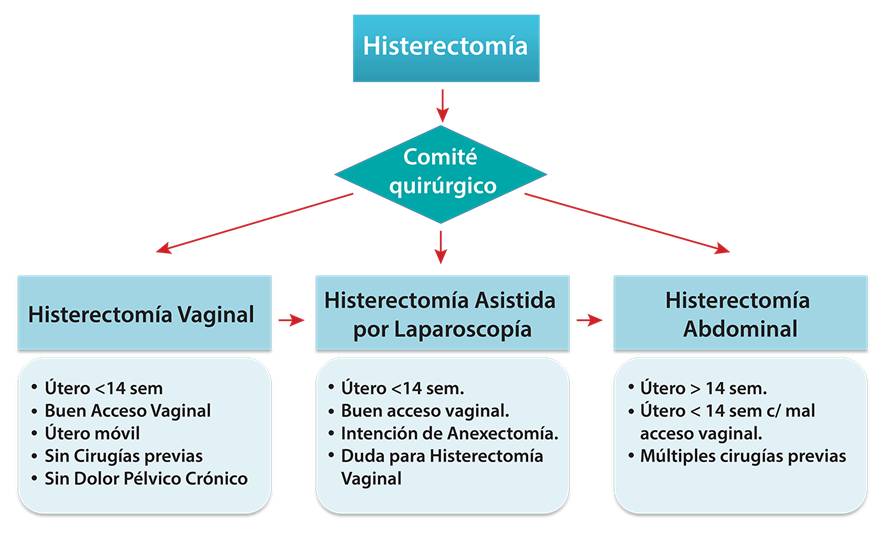
El ACOG sugiere que la vía para realizar una histerectomía debe ser acorde a las características de la paciente y a la experiencia del cirujano. Sin embargo, de acuerdo a las casuísticas publicadas por diferentes grupos de trabajo, ha sido solo la experiencia del cirujano la que ha prevalecido en la toma de decisión, motivando la necesidad de comparar los resultados de cada técnica evaluando distintos parámetros. De esta manera se han realizado muchas publicaciones las cuales fueron revisadas (16) y en donde -luego de evaluar recuperación, complicaciones, satisfacción de la paciente y gastos asociados- se concluye que toda vez que es posible se debe realizar una HV, en segunda opción HVAL y finalmente HA. La HVAL tiene un rol como ayuda a una HV, sobretodo en pacientes con cirugías previas, historia de dolor pélvico crónico o cuando se desee realizar SOB. No obstante, se reconoce la existencia de grupos quirúrgicos con gran experiencia en HL que pueden demostrar similares resultados con excepción de los costos asociados.
Otro aspecto interesante, y que ha sido motivo de discusión, es el referido a la Histerectomía Subtotal (HS). Esta cirugía tiene como gran ventaja -al compararla con HA total- que tiene menos complicaciones: daño ureteral, vesical, hemorragias y posibilidad de transfusión e infecciones además de ofrecer no dañar estructuras de sostén y piso pélvico, evitando prolapsos e incontinencia de orina de esfuerzo. Como no acorta vagina y no deja una cicatriz en ella, también era posible plantear que aquellas pacientes sometidas a esta cirugía tendrían mejor calidad en su actividad sexual, comparadas con aquellas sometidas a una HA total. Sin embargo una revisión del Cochrane en este sentido (17), demuestra que no existen diferencias entre la HA total e HS al evaluar parámetros urinarios, digestivos y sexuales. Es decir la indicación actual de la Histerectomía Subtotal es solamente evitar complicaciones en pacientes que ofrecen mayor dificultad desde el punto de vista técnico.
Propuesta de manejo del SUA (Algoritmo)
El esquema propuesto aplica para aquellas mujeres con SUA mayor a 3 meses, de acuerdo a recomendación FIGO. Debe considerarse en todo momento los deseos de fertilidad futura de la paciente. Se debe comenzar con evaluación clínica completa y estudio básico hematológico para ver repercusión del SUA en hematocrito-hemoglobina y descarte de coagulopatías. En líneas generales, es indispensable en la evaluación identificar a aquellas mujeres con patología orgánica focal para ofrecerles un tratamiento acorde. Si esto no se logra, se debe continuar con los tratamientos farmacológicos validados en la actualidad, con plazos determinados. Si este manejo fracasa se debe continuar con las alternativas quirúrgicas: Histerectomía, de preferencia por vía vaginal.
Desde el punto de vista diagnóstico, el manejo actual involucra la evaluación clínica acompañada de una ECO TV, HCP y biopsia directa o dirigida. Si no se cuenta con HCP debe realizarse una HSG y toma de biopsia dirigida. Otra buena alternativa es evaluación clínica más ECO 3D con biopsia dirigida o bien evaluación clínica más HSG 3D con su respectiva biopsia. Este manejo permite identificar las causas focales del SUA y por lo tanto seleccionar a aquellas pacientes que se beneficiarán de un tratamiento conservador. (Figura 1)
Figura 1 Algoritmo de tratamiento SUA
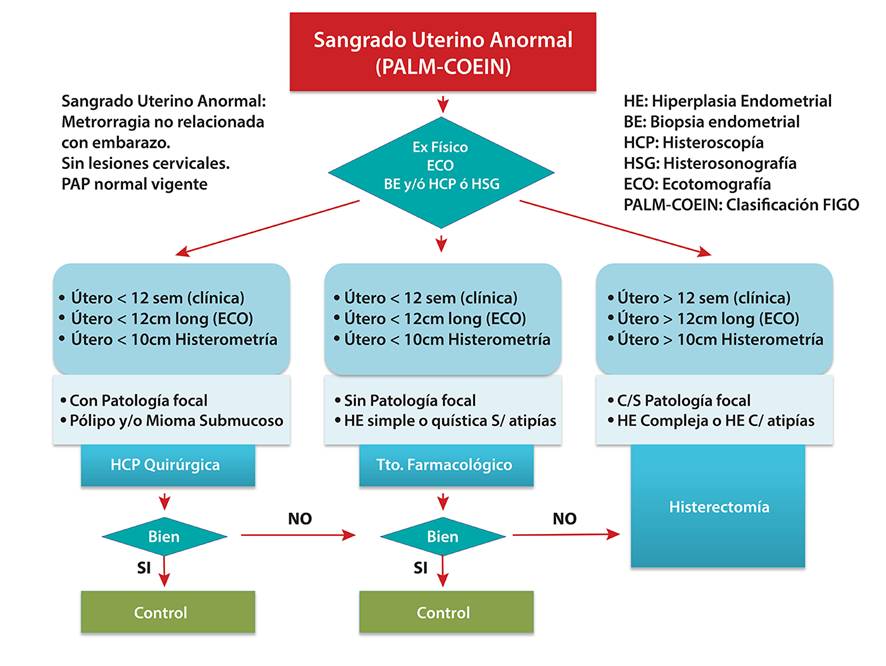
El tratamiento de SUA con medicamentos está indicado en úteros de mediano tamaño, en los cuales no se ha identificado una patología focal, con excepción de hiperplasias endometriales sin atipias. De acuerdo a la evidencia existente, la primera opción de tratamiento es ácido tranexámico en episodios puntuales o DIU-LNG como tratamiento prolongado. Como segunda opción es posible utilizar AINE o ACO o progestágenos de depósito, este último en caso de hiperplasia endometrial sin atipia. Si se inicia tratamiento con ácido tranexámico, ACO y/o AINE, se debe evaluar en tres meses. Si no hay mejoría y se cumplen los criterios de inclusión y exclusión, se debe continuar con DIU-LNG. Los resultados del DIU-LNG, siempre y cuando las condiciones de la paciente lo permitan, no deben ser evaluados antes de 6 meses. Si estos tratamientos y tiempos planteados no logran controlar adecuadamente el SUA es necesario continuar con las alternativas siguientes. (Figura 2)
Figura 2 Tratamiento farmacológico en SUA
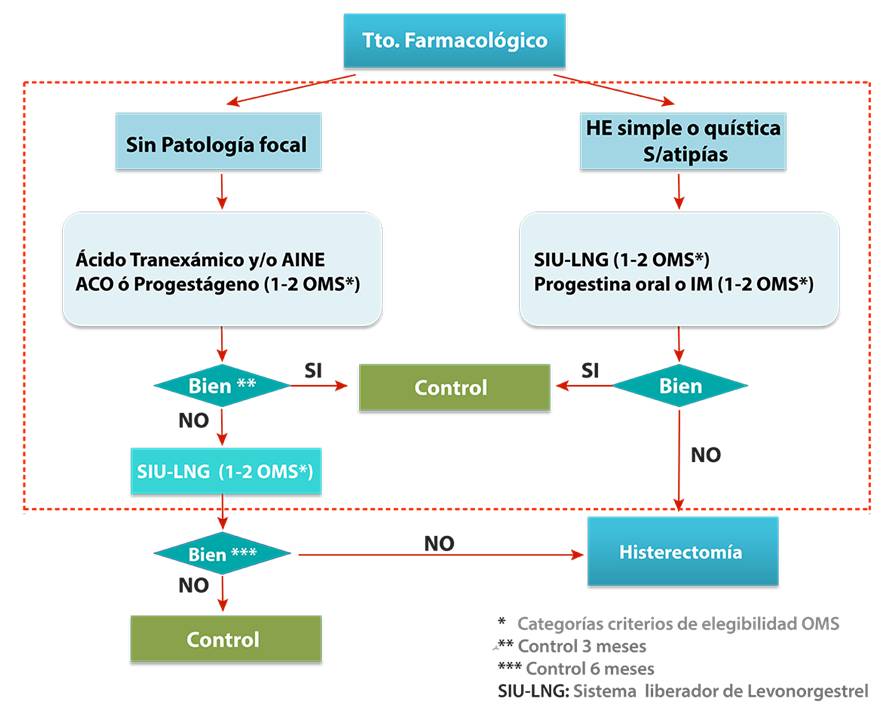
El manejo quirúrgico conservador está centrado en el uso del resectoscopio como tratamiento de tumores intracavitarios en úteros de mediano volumen. Posterior a esta cirugía se evalúan resultados y en caso de persistencia de SUA se maneja con tratamiento farmacológico siguiendo esquema del párrafo anterior, incluida la posibilidad del DIU-LNG. Puesto que los tumores intracavitarios aumentan el riesgo de expulsión de DIU-LNG es conveniente primero la resección de ellos vía histeroscópica.
La histerectomía es el tratamiento definitivo del SUA. Sin embargo, es un procedimiento quirúrgico que implica diversos riesgos. Para llegar a cualquiera de las alternativas de histerectomía es necesario tener una apropiada indicación y cumplir con el manejo propuesto, con excepción de úteros de gran volumen o numerosos miomas sintomáticos los cuales no responderán a tratamientos médicos o cirugías conservadoras. (Figura 3, 4)
Figura 3. Tratamiento quirúrgico no conservador en SUA
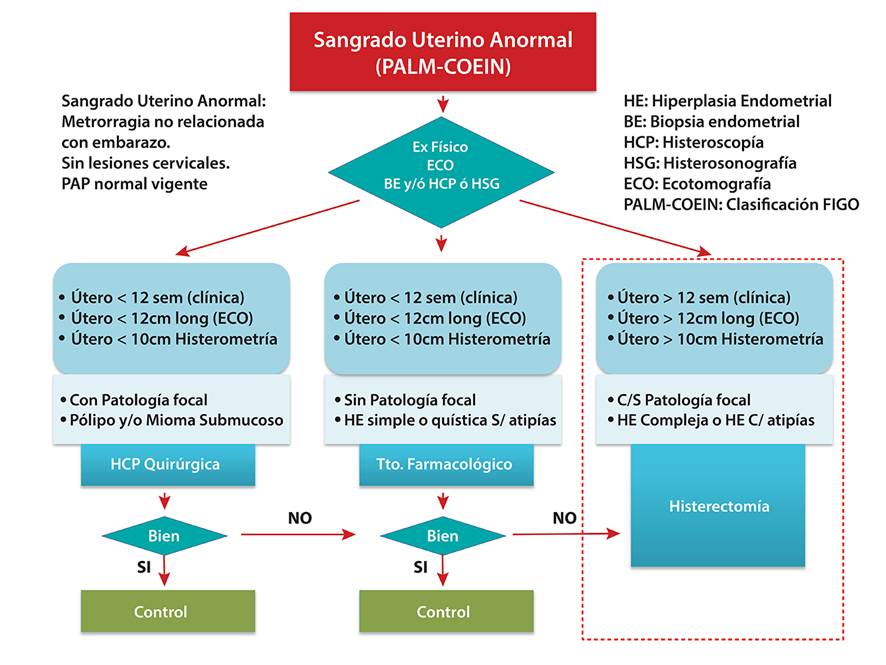
Figura 4 Vía de la Histerectomía
Análisis fármaco-económico del DIU-LNG en el manejo del SUA
El análisis costo efectividad (ACE) es una herramienta central en las estrategias de micro-gestión de la oferta, que adquiere gran relevancia en la contención de costos en salud, gran preocupación de los Sistemas de Salud a nivel mundial.
Un ACE comienza con el enunciado del problema, para luego continuar con una exhaustiva revisión de los resultados de las alternativas a comparar, obtenidos de medicina basada en evidencia. Posterior a ello se realiza la recopilación de datos con miras a obtener el costo de las intervenciones, se establece la relación costo/efectividad, se realiza análisis de sensibilidad para comprobar resultados, y finalmente se elaboran las conclusiones y recomendaciones. Lo que busca el ACE no es necesariamente que se gaste menos, sino que se gaste mejor. Busca la eficiencia del gasto en relación a los resultados.
Las cuatro metodologías básicas del ACE son: costo-minimización, costo- efectividad propiamente tal, costo-utilidad y costo-beneficio.
En el ACE costo-minimización solo se comparan costos, y es posible realizarlo siempre y cuando los resultados a comparar de las alternativas sea el mismo. Como los resultados son los mismos solo se opta por elegir aquella alternativa de menor costo. Por esta razón su aplicación es muy limitada. En las tres metodologías restantes se incorpora la variable resultado creando los cuadrantes del ACE (Figura 5).
Figura 5 Plano del análisis costo efectividad
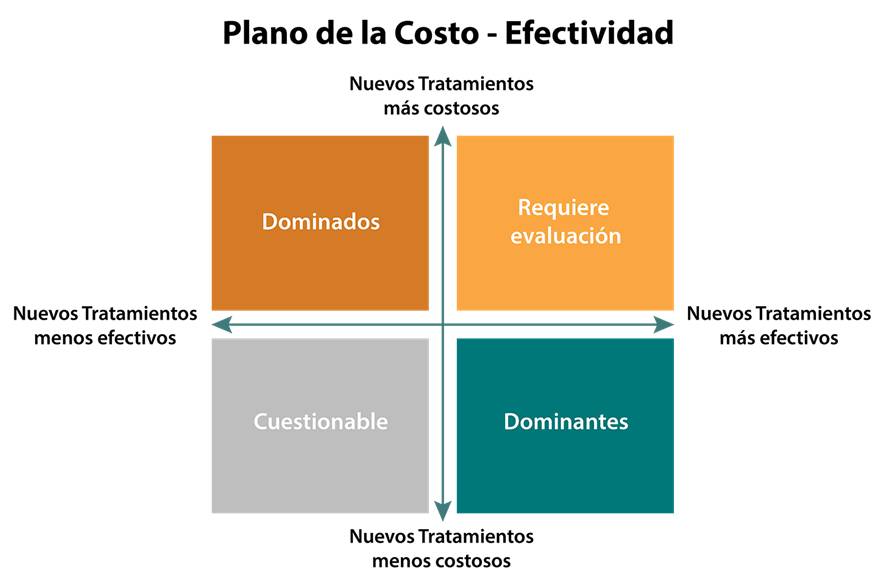
Las intervenciones médicas (tratamiento, cirugía, etc.) menos costosas y más efectivas son llamadas Dominantes frente a la alternativa comparada y deben ser incorporadas sin mayor análisis. Las intervenciones más costosas y menos efectivas son llamadas Dominadas y deben ser excluidas sin mayor análisis. Las menos costosas pero menos efectivas (Cuestionable) y las más costosas pero más efectivas, son las que justifican un ACE detallado.
En el ACE, costo-efectividad, se dividen los costos expresados en $ por el resultado expresado en unidades naturales (por ejemplo, éxito de un determinado tratamiento, número de embarazos evitados, número de histerectomías evitadas, etc). Permite evaluar distintas alternativas con distintos resultados.
En el ACE, costo-utilidad, se dividen los costos expresados en $ por el resultado expresado en medidas de utilidad. La medida de utilidad más ampliamente usada es el QALY (Quality Adjusted Life Years) que mide los años de vida ajustados por calidad. Los años de vida se ajustan por un ponderador de calidad el cual se obtiene de cuestionarios validados. El cuestionario más utilizado es el EQ-5D. Un QALY es un año de vida en óptimas condiciones de salud. Este análisis permite comparar alternativas en distintas áreas de la medicina. Por ejemplo se pueden comparar alternativas que generen más QALYs entre distintas especialidades.
En el ACE costo-beneficio, se dividen los costos expresados en $ por el resultado expresado también en $. Este es un análisis aún más amplio, que permite comparar en forma intersectorial distintas alternativas o estrategias que pueden ir más allá del ámbito de la salud.
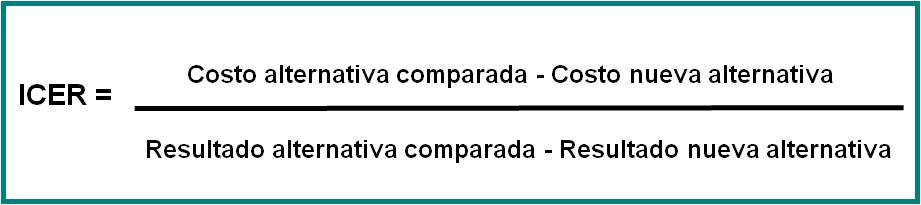
Los resultados pueden estar expresados por su relación costo/efectividad ó mejor aún por ICER (Incremental Cost Efectivity Ratio) que es el índice incremental de las alternativas analizadas, y que se obtiene al restar los costos de las alternativas divididos por la diferencia de los resultados (Figura 6). Las alternativas mejores son aquellas que obtenga un menor ICER en relación a una alternativa estudiada.
Figura 6 Costo-efectividad incremental (incremental cost efectivity ratio)
Estudios de ACE con DIU-LNG en el manejo del SUA
Uno de los primeros estudios en que se realiza ACE con DIU-LNG (Mirena®, Bayer) es el publicado por Hurskainen y cols en JAMA 2004 (18). En este estudio clínico randomizado se evaluó la histerectomía (n=115) versus DIU-LNG (n=117) luego de 5 años de seguimiento, en pacientes en lista de espera para histerectomía, registrando los costos directos e indirectos en cada grupo y los resultados en término de QALYs obtenidas por EQ-5D.
En el análisis de costo se incluyeron los costos directos de uso de servicio hospitalario (costos de la hospitalización, procedimientos, consultas pre y post intervención, y medicamentos) y los costos indirectos (días de enfermedad y pérdida de productividad). Como parte del estudio se incorporaron los costos directos e indirectos relacionados con complicaciones en el grupo de pacientes sometidas a la histerectomía en forma inicial y los costos directos e indirectos por menorragia (consultas, medicamentos, trasporte, etc) en el grupo de pacientes con DIU-LNG, en los años de seguimiento.
Del grupo de pacientes con DIU-LNG solo el 42 % de ellas fue histerectomizada finalmente, incorporando los costos de la intervención y sus complicaciones en este grupo. De aquellas que tenían DIU-LNG in situ al cabo de los 5 años, 75% de ellas estaban en amenorrea u oligomenorrea, 19% con sangrado irregular y 6% con sangrado escaso.
Los resultados en términos de QALYs obtenidas por EQ-5D y de satisfacción usuaria, no demostraron diferencias significativas entre los grupos estudiados durante el periodo evaluado. De esta manera y con iguales resultados no se realizó determinación de ICER. Por lo tanto, el análisis realizado es un ACE de tipo costo-minimización. El costo total promedio del grupo de pacientes de DIU-LNG, incluido el costo de la histerectomía en aquellas pacientes sometidas finalmente a esta intervención, fue un 39,5% más bajo que el costo total promedio de las pacientes sometidas a histerectomía como intervención inicial (US$ 2.817 grupo DIU-LNG versus US$ 4.660 grupo histerectomía), luego de 5 años de seguimiento.
El National Institute for Health and Clinical Excellence (NICE), institución dependiente del NHS Británico, publicó en 2007 una extensa revisión (10), con 606 citas bibliográficas, y un detallado ACE evaluando todas las alternativas existentes para el manejo del Sangrado Menstrual Abundante (SMA). En esta revisión se analizó los resultados publicados para todas las alternativas, y se indexó con su respectivo nivel de evidencia, elaborando pautas con grados de recomendación. Fueron evaluados: ácido mefenámico, ácido tranexámico, anticonceptivos orales combinados, DIU-LNG, métodos ablativos de primera y segunda generación e histerectomía.
En anexo fármaco-económico de estas guías se presenta ACE con una simulación mediante modelo de Markov. Este modelo es ampliamente usado y validado en estudios de costo efectividad y consiste en utilizar algoritmos elaborados por medicina basada en evidencia para el manejo de una determinada patología, con las probabilidades de éxito de cada acción, e introducir un número virtual de pacientes, generalmente 1000, simulando resultados en término de costos y efectividad.
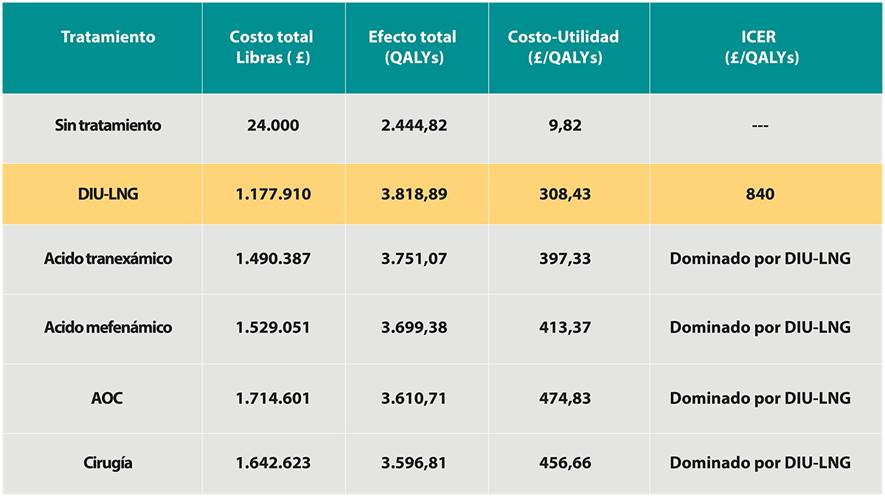
En las guías NICE el ACE se realizó considerando QUALYs como resultado. Por lo tanto, este es un estudio costo-utilidad. Destaca de estas guías que todas las alternativas, sean estas tratamientos farmacológicos o quirúrgicos, son dominadas por DIU-LNG. Dicho de otra manera, DIU-LNG está en cuadrante dominante: es menos costoso y más efectivo. De acuerdo a la conclusión de estas guías, es el tratamiento de primera línea del SMA (Tabla 2)
Tabla 2 Resumen de ACE de todos los tratamientos para Sangrado Menstrual Abundante en 1000 mujeres en 5 años. NICE 2007
Una publicación española (19), del tipo costo-efectividad y también del tipo costo-utilidad, usando modelo de Markov, con cohorte hipotética de pacientes y evaluando a anticonceptivos orales combinados (AOC), progestágenos cíclicos (PROG) y DIU-LNG en el SMA, con un horizonte de 5 años, demostró la dominancia de DIU-LNG en relación a las otras dos alternativas farmacológicas. Las medidas naturales de efectividad utilizadas fueron: meses libre de síntomas (SFM) y meses logrados sin cirugía (SuFM). La medida de utilidad usada fue una derivación del QALY, que en vez de ser años ajustados por calidad de vida fue de meses ajustados por calidad de vida (QALMs) obtenidas por encuesta tipo EQ-5D, donde 1 QALM es un mes en óptimas condiciones de salud. DIU-LNG resultó dominante sobre AOC y PROG (menos costoso y más efectivo) en las evaluaciones costo-efectividad y costo-utilidad.
Luego de los análisis costo efectividad, se realizó análisis de sensibilidad para la costo-utilidad, demostrándose que aún al cambiar datos sensibles de las variables estudiadas, DIU-LNG continua teniendo la mejor relación costo efectiva (Figura 7). Este trabajo de fármaco-economía coincide con la recomendación de la Sociedad Española de Ginecología y Obstetricia: DIU-LNG debe ser tratamiento de primera línea en SMA en guías clínicas españolas.
Figura 7 Plano Costo-efectividad de 10.000 pacientes simuladas en estudio español
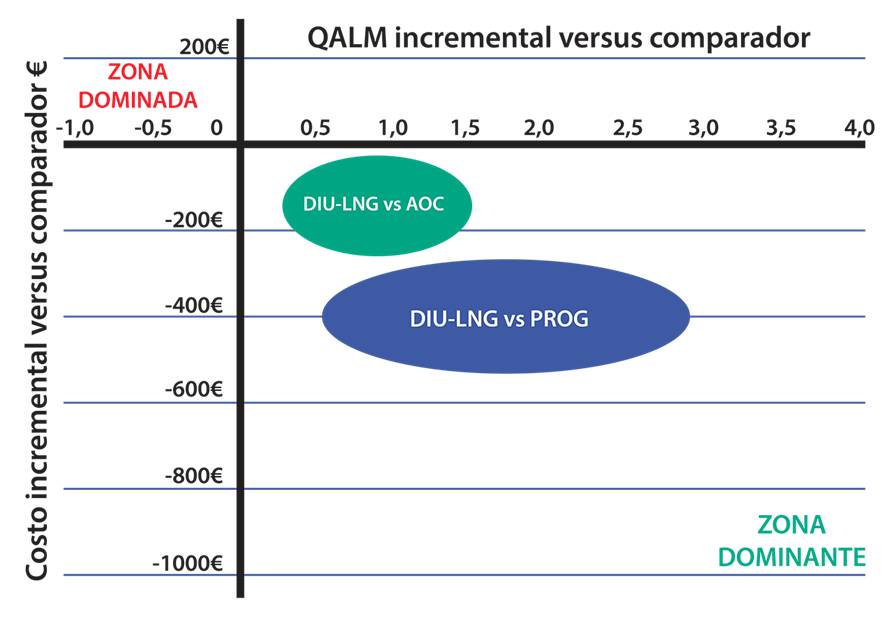
Resultado de análisis de sensibilidad: DIU-LNG con ICER negativo al compararlo con AOC (casos en óvalo verde). DIU-LNG con ICER negativo al compararlo con PROG (casos en óvalo azul). Adaptado de Lete I. et al. Eur J Obstet Gynecol (2010)
En Chile existen 2 trabajos aún no publicados. En el primero de ellos se realizó un sencillo ACE de DIU-LNG versus Ablación endometrial termal con Thermachoice® (20), utilizando la probabilidad de éxito de cada una de las alternativas, obtenida de revisión de literatura (número de histerectomías evitadas como medida natural). Se efectuó simulación con 100 pacientes, determinando costos de cada una, incluyendo su fracaso y posterior histerectomía. En este ACE de tipo costo-efectividad, DIU-LNG demostró tener una mejor relación costo-efectividad: 49% menor al comparar con Thermachoice®. Un segundo trabajo, aún en curso, utilizando también histerectomías evitadas como resultado, es decir nuevamente ACE de tipo costo-efectividad, está demostrando la utilidad clínica y económica de DIU-LNG como alternativa a la histerectomía en pacientes con alto riesgo quirúrgico.
En conclusión, todos los trabajos análisis costo efectividad de DIU-LNG en SUA, sean costo- minimización, costo-efectividad o costo-utilidad, demuestran en forma coincidente e incuestionable que el DIU-LNG es la mejor alternativa costo-efectiva. Por esta razón, EL DIU-LNG es tratamiento de primera línea en SMA en guías NICE y de Finlandia. Toda esta evidencia debiera ser considerada en nuestros países para mejorar el acceso al DIU-LNG.
Bibliografía
-
Munro MG, Critchley HOD, Fraser IS for the FIGO Menstrual Disorders Working Group. Fertile Steril 2011; 95 (7): 2204-2208.
-
Escobar D, Alvarado C, Bueno F. Análisis comparativo entre ultrasonografía transvaginal e histeroscopía diagnóstica en patología endouterina. Rev Chil Obstet Ginecol 2000; 65(3): 183-187.
-
Smith J, Schulman H. Current dilatation and curettage practice: A need for revision. Obstet Gynecol 1985; 65: 516-518.
-
Lethaby A, Farquhar C, Cooke I. Antifrinolíticos para el sangrado menstrual abundante (Revisión Cochrane traducida). Biblioteca Cochrane Plus, número 2, 2006.
-
Lethaby A, Augood C, Duckitt K. Fármacos antiinflamatorios no esteroidales para la menorragia. (Revisión Cochrane traducida). Biblioteca Cochrane Plus, número 2, 2006.
-
Lethaby A, Irvine G, Cameron I. Progestágenos cíclicos para el sangrado menstrual abundante. (Revisión Cochrane traducida). Biblioteca Cochrane Plus, número 2, 2006.
-
Valdés P, Sánchez R. Dispositivos intrauterinos con levonorgestrel. Una nueva alternativa terapéutica en el sangrado uterino anormal de origen orgánico. Rev Chil Obstet Ginecol 2004; 69 (1): 35-38.
-
Escobar D, Alvarado C, Valdés P, Varas C. Uso de DIU-LNG como alternativa a la histerectomía en pacientes de alto riesgo quirúrgico. Rev Chil Obstet Ginecol 2007; 70 (4):217-221.
-
Lethaby A, Cooke I, Rees M. Progestrone or progestagen-releasing intrauterine systems for heavy menstrual bleeding (Cochrane review). Cochrane Library, Issue 3, 2006.
-
NICE 2007 Clinical guideline 44. Heavy menstrual bleeding. Developed by the National Collaborating Centre for Women’s and Children’s Health. NHS. Published by the RCOG Press at the Royal College of Obstetricians and Gynaecologists. (www.nice.org.uk/CG044).
-
Janssen C, Scholten P, Heintz P: A simple visual assessment technique to discriminate between menorrhagia and normal menstrual blood loss. Obstet Gynecol 1995; 85: 977-982.
-
Escobar D, Alvarado C, Schwarze J. Resección de pólipos y miomas por vía histeroscópica. Rev Chil Obstet Ginecol 1999; 64(1): 15-20.
-
Alvarado C, Escobar D, Barros J, Gonzalez R, Corvetto M. Resección Endometrial Transcervical: Una alternativa a la Histerectomía. Rev Chil Obstet Ginecol 2002; 67 (6): 456-460.
-
Lethaby A, Hickey M, Garry R. Técnicas de destrucción endometrial para la menorragia. (Revisión Cochrane traducida). Biblioteca Cochrane Plus, número 2, 2006.
-
Kaunitz, Meredith, Inki et al. LNG-IUS & Endometrial ablation. Systematic review and meta-analysis. Obstetrics & Gynecology. 2009 (5): 1104-1116
-
Johnson N, Barlow D, Lethaby A, Travender E, Curr E, Garry R. Abordajes quirúrgicos para la histerectomía por enfermedades ginecológicas benignas. (Revisión Cochrane traducida). Biblioteca Cochrane Plus, número 2, 2006.
-
Lethaby A, Ivanova V, Johnson N. Total versus subtotal hysterectomy for benign gynaecological conditions (Cochrane review). Cochrane Library, Issue 2, 2006.
-
Hurskainen R. et al. Clinical outcomes and costs with the Levonorgestrel-releasing intrauterine system or hysterectomy for treatment of menorrhagia. Randomized trial 5-Year follow-up. JAMA, 2004. Vol 291, No. 12.
-
Lete I. et al. Economic evaluation of the levonorgestrel-releasing intrauterine system for the treatment of dysfunctional uterine bleeding in Spain. Eur J Obstet Gynecol (2010).
-
Escobar D. et al. Ensayo: Análisis costo efectividad del uso de DIU-LNG versus Ablación endometrial termal como alternativa a la histerectomía. Diplomado en gestión de organizaciones e instituciones de salud 2010. Universidad Andrés Bello.



